Սովորել՝ Ատոմի կառուցվածքը։ Էլեկտրոն և միջուկ։
Թեմա- Իզոտոպներ։
Էջ՝ 92-101
Իզոտոպ, զանգվածային թիվ, հարաբերական ատոմային զանգված
Միևնույն քիմիական տարրի ատոմների տարրատեսակները, որոնք ունեն միջուկի նույն լիցքը, բայց տարբեր զանգվածային թվեր, կոչվում են իզոտոպներ:
Իզոտոպների գոյությունը բացահայտվել է դեռևս 1906 թ, իսկ հիմնավին հաստատվել և ուսումնասիրվել է 1920թ:
Իզոտոպը բնութագրվում է երկու մեծությամբ (RZA).
- Z-միջուկի դրական լիցք — գրվում է քիմիական նշանի ձախ-ներքևի մասում,
- A-զանգվածային թիվ — գրվում է ձախ-վերևի մասում:
Բառացի «իզոտոպ» նշանակում է՝ իզո-հավասար, նույն և տոպ— տեղ, այսինքն՝ նույն տեղը:
Իզոտոպները ներկայացվում են տարբեր ձևերով: Օրինակներ՝

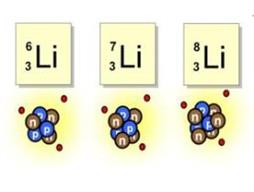
Նեյտրոնների թիվը միջուկում հաշվում են հետևյալ բանաձևի միջոցով՝ N=A−Z
Խնդիրներ ինքնուրույն լուծման համար
1.Որքա՞ն են պրոտոնների, նեյտրոնների և էլեկտրոնների քանակները 9 կարգաթվով ու 19 զանգվածային թվով քիմիական տարրի ատոմում։ Ո՞ր քիմիական տարրն է դա:
Պատ. ՝ 9,10,9,F:
2.Բնության մեջ քլորը (CI) հանդիպում է երկու իզոտոպի ձևով, որոնցից մեկը 35CI է՝ 77,5 % մոլային բաժնով: Ո՞րն է մյուս իզոտոպը, եթե քլորի միջին ատոմային զանգվածը 35,45 է։
Պատ.՝ 37СІ:
ՀԱՐՑԵՐ ԵՎ ՎԱՐԺՈՒԹՅՈՒՆՆԵՐ
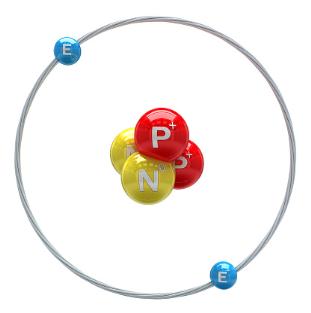
1.Ի՞նչ մասնիկներից է կազմված ատոմի միջուկը, և ինչո՞վ են նրանք տարբերվում մեկը մյուսից:
Ատոմի միջուկը կազմված է պրոտոններից և նեյտրոններից: Պրոտոնի լիցքը բացարձակ արժեքով հավասար է էլեկտրոնի լիցքին։ Այն դրական է լիցքավորված։ Իսկ նեյտրոնը չեզոք լիցք ունեցող տարրական մասնիկ է, որը կազմում է ատոմի միջուկը։
2.Ատոմի վերաբերյալ ո՞ր պնդումն է ճիշտ: Ատոմը կազմված է.
ա) միջուկից և էլեկտրոններից✅
բ) պրոտոններից և էլեկտրոններից
գ) պրոտոններից և նեյտրոններից
դ) նեյտրոններից և էլեկտրոններից
3.Ինչի՞ է հավասար տվյալ ատոմի միջուկի լիցքը.
ա) 0
բ) +1
գ) այդ տարրի ատոմային համարին պարբերական համակարգում
դ) տարրի հարաբերական ատոմային զանգվածին✅
4.Որքա՞ն է պրոտոնի լիցքը.
Ա)+1✅
Բ)-1
Գ)0
5.Ինչի՞ է հավասար նեյտրոնի լիցքը.
ա) -1
բ) +1
գ)0✅
դ) Ζ
6.Ինչպե՞ս կարելի է որոշել նեյտրոնների թիվն ատոմի միջուկում, եթե հայտնի են վերջինիս լիցքն ու զանգվածային թիվը:
Միջուկում նեյտրոնների թիվը հավասար է միջուկի զանգվածային թվի և պրոտոնների թվի տարբերությանը:
N=A−Z
7.Ո՞րն է առավելագույն թվով բնական իզոտոպներ ունեցող տարրը։
Առավելագույն թվով բնական իզոտոպներ ունեցող տարրն անագն է։ Այն 10 իզոտոպի խառնուրդ է։
8.Ինչո՞վ է տարբերվում դեյտերիումը «սովորական» ջրածնից, ծանր ջուրը (D_{2}*O) սովորական ջրից (H2O):
Դեյտերիումը պարունակում է մեկ պրոտոն և մեկ նեյտրոն։ Նրա ատոմային զանգվածն ավելի մեծ է, քան ջրածնինը։ Այսպիսով՝ ջրածնի միջուկը կազմված է 1 պրոտոնից, դեյտերիումինը՝ 1 պրոտոնից և 1 նեյտրոնից:

9.Ինչո՞վ են տարբերվում 35 CI և 37CI իզոտոպները.
1) միջուկի լիցքի մեծությամբ
2) միջուկում առկա պրոտոնների թվով
3) էլեկտրոնների թվով
4) միջուկում առկա նեյտրոնների թվով✅
(Տվյալ քիմիական տարրի իզոտոպները ատոմային միջուկի վրա ունեն նույն լիցքը, այսինքն՝ նույն ատոմային թիվը և զբաղեցնում են նույն տեղը պարբերական համակարգում, ունեն նույն թվով պրոտոններ ատոմային միջուկում, բայց տարբերվում են միմյանցից նեյտրոնների թվով։ Այսպիսով, 35 Cl իզոտոպի ատոմային միջուկը պարունակում է 17 պրոտոն, քանի որ քլորի սերիական համարը 17 է և 18 նեյտրոն (35-17 = 18), իսկ 37 Cl իզոտոպի միջուկը պարունակում է 17 պրոտոն և 20 նեյտրոն։ (37-17 = 20)։)
10.Ո՞ր շարքում է ճիշտ ներկայացված K իզոտոպում առկա պրոտոնների, էլեկտրոնների և նեյտրոնների թիվը՝ համապատասխանորեն.
1) 19, 19, 19
2) 19, 19, 20✅
3) 19, 20, 19
4) 19, 19, 18